
การทดลองทางเทคนิคอย่างง่าย ๆ มีประโยชน์มากสำหรับเด็ก ๆ นี่คือการใช้เวลาร่วมกันและการปลูกฝังทักษะและความเข้าใจโดยนักออกแบบขนาดเล็กพื้นฐานที่ก้อนนั้นเหมือนในการ์ตูนที่มีชื่อเสียงไม่ได้เติบโตบนต้นไม้
คราวนี้เราตัดสินใจที่จะสร้างแหล่งเคมีที่ง่ายที่สุดและลองใช้กับสิ่งที่ใช้งานได้จริง เมื่อพูดถึงการใช้งานจริงมันก็คุ้มค่าที่จะนึกถึงว่าเมื่อไม่กี่ชั่วอายุคนที่ผ่านมานักวิทยุสมัครเล่นเพื่อจัดหาเครื่องรับและส่งสัญญาณวิทยุแบตเตอรี่ได้ถูกเสนอให้ผลิตเซลล์กัลวานิกหรือแบตเตอรี่หลายชนิดเพื่อการผลิตอิสระ นี่คือองค์ประกอบของ Leklanshe และ Popov [1] หน้า 9 ... 18 หรือแบตเตอรี่ตะกั่วโปแตชหรือแก๊ส [1], หน้า 22 ... 28 องค์ประกอบที่มีกระแสไฟฟ้าค่อนข้างสูงหลายตัวเชื่อมต่อกับหลอดไส้ (ไส้หลอดของหลอดวิทยุ) องค์ประกอบเล็ก ๆ หลายสิบตัวเข้ากับแบตเตอรี่แอโนดแรงดันไฟฟ้าที่สามารถถึง 60-80 โวลต์ แบตเตอรี่นั้น“ เปียก” - พร้อมอิเล็กโทรไลต์ของเหลวและจำเป็นต้องได้รับการดูแลและบำรุงรักษา
ดังนั้น เซลล์กัลวานิคคำสองสามคำ“ อย่างไร” และ "ทำไม" กระแสไฟฟ้าเกิดขึ้นเมื่อโลหะมีปฏิกิริยา ในกรณีนี้จะมีความต่างศักย์ (แรงดันไฟฟ้า) แตกต่างกันเกิดขึ้น ย้อนกลับไปในปี ค.ศ. 1793 อเลสซานโดรโวลตาสร้างเซลล์กัลวานิค (ขั้วโวลต้า) สร้างกิจกรรมสัมพัทธ์ของโลหะที่รู้จักแล้ว: Zn, Pb, Sn, Fe, Cu, Ag, Au "ความแข็งแกร่ง" ของเซลล์กัลวานิกนั้นยิ่งใหญ่กว่ามากยิ่งห่างจากโลหะในแถวนี้มากเท่าไหร่ (ชุดแรงดันไฟฟ้า)

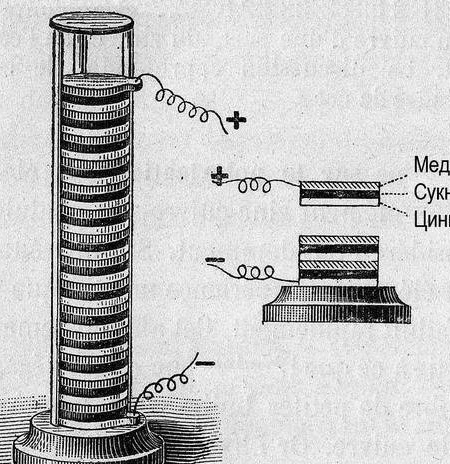
ต่อมาในการจัดระเบียบข้อมูลศักยภาพของ“ ไฮโดรเจนอิเล็กโทรด” ถูกนำไปอ้างอิงเป็นศูนย์ หลังจากการวัดศักยภาพของโลหะที่จับคู่กับเขาโลหะการทดลองจะถูกจัดเรียงเป็นแถว ตารางผลลัพธ์นั้นถูกเรียกว่า "ชุดแรงดันไฟฟ้าของโลหะ" และในห้องเคมีจะต้องติดกับระบบธาตุและภาพเหมือนของมิทรีอีวานโนวิช
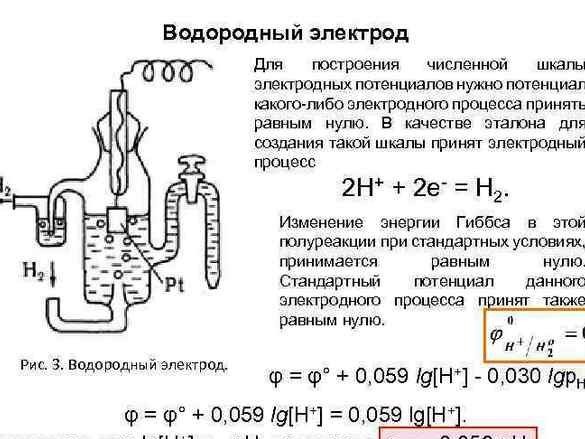

ความเค้นจากโลหะจำนวนมากเป็นสิ่งที่มีประโยชน์ในกรณีของเราเช่น Alessandro Volta จะรู้ว่ายิ่งโลหะถูกแยกออกจากกันมากเท่าไหร่ความตึงเครียดก็จะยิ่งเพิ่มมากขึ้นเท่านั้น
ในการทดลองของเราเช่นคลาสสิกเราใช้ทองแดงและสังกะสีเมื่อแผ่นถูกแช่อยู่ในอิเล็กโทรไลต์ระหว่างมันกับแผ่นสังกะสีจะเกิดปฏิกิริยาทางเคมีขึ้นมาเนื่องจากประจุลบสะสมบนแผ่นและมีประจุลบ จากการที่ปฏิกิริยาเกิดขึ้นในเซลล์กัลวานิคอิเล็กโทรดสังกะสีจะค่อยๆสลายไป
ในอิเล็กโทรดทองแดงในระหว่างการทำงานของเซลล์กัลวานิกนั้นจะเกิดฟองไฮโดรเจนเล็ก ๆ ขึ้นที่แยกผิวทองแดงออกจากอิเล็กโทรไลต์ ปรากฏการณ์นี้เรียกว่าในเซลล์กัลวานิคมันเป็นอันตรายพวกมันกำลังดิ้นรนกับมัน ในการกำจัดไฮโดรเจนที่ปล่อยออกมาสารที่เรียกว่าไฮโดรเจนจะถูกนำเข้าไปในอิเล็กโทรไลต์ ในบทบาทของพวกเขามักจะมีสารประกอบของแมงกานีสคอปเปอร์ซัลเฟต ในการทดลองง่าย ๆ โพแทสเซียมเปอร์แมงกาเนตสามารถใช้ในร้านขายยาได้
สิ่งที่เราใช้สำหรับการทดสอบ
อุปกรณ์และวัสดุ
สำหรับการประกอบของเซลล์กัลวานิกเช่นอิเล็กโทรดทองแดงคุณสามารถใช้ลวดลวดฟอยล์ สังกะสีสามารถสกัดได้จากองค์ประกอบแห้งสามารถใช้ผลิตภัณฑ์ชุบสังกะสี แทนที่จะเป็นสังกะสีคุณสามารถลองใช้อิเล็กโทรดของอลูมิเนียมหรือเหล็ก โซเดียมคลอไรด์สำหรับอิเล็กโทรไลต์ซึ่งเป็นสายไฟอ่อน ๆ คุณต้องใช้โวลต์มิเตอร์หรือมัลติมิเตอร์คีมตัดและกรรไกร ในฐานะภาชนะสามารถใช้ภาชนะที่ไม่ใช่โลหะที่มีขนาดเหมาะสมได้ แก้วสะดวกกว่าถ้วยพลาสติกน้ำหนักเบา - หนักกว่ามีความเสถียรมากกว่าและกระแทกยากกว่า เป็นสิ่งที่ดีมากหากมีแรงดันไฟฟ้าต่ำกระแสต่ำ - วิทยุง่าย ๆ นาฬิกาควอทซ์ ฯลฯ
แบตเตอรี่ "แรงดันสูง" ของลวดและสกรู
ด้วยความเรียบง่ายของรายละเอียดและแรงดันไฟฟ้าค่อนข้างสูงที่ได้รับเราพยายามรวบรวมแบตเตอรี่ดังกล่าว คู่ของโลหะ“ คลาสสิค” - ทองแดง - สังกะสี - ถูกนำมาใช้ที่นี่ ความคิดคือการใช้ตัวยึดสังกะสีเป็นอิเล็กโทรดสังกะสี อย่างงดงาม เป็นที่ชัดเจนว่าองค์ประกอบดังกล่าวไม่ได้ถูกออกแบบมาสำหรับการทำงานในระยะยาว - ชั้นบาง ๆ ของสังกะสีจะละลายอย่างรวดเร็วอย่างไรก็ตามสิ่งนี้ไม่สำคัญสำหรับการทดลองระยะสั้น แต่สกรูชุบสังกะสีหรือฟันเฟืองนั้นเต็มไปหมด
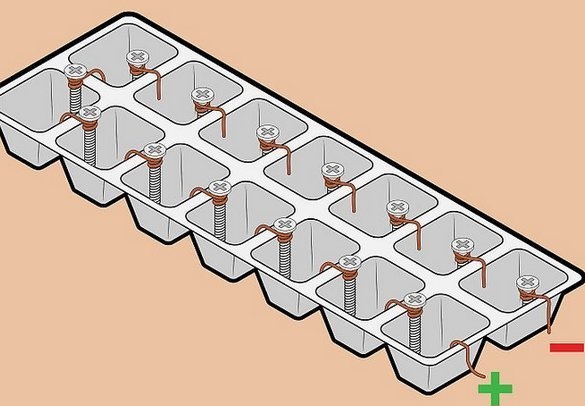
ลวดยังใช้เป็นอิเล็กโทรดทองแดง - นอกจากนี้ยังเป็นวัสดุที่มีอยู่อย่างกว้างขวางนอกจากนี้ - การติดตั้งองค์ประกอบที่สะดวกที่สุดในแบตเตอรี่ - องค์ประกอบทั้งหมดมีการเชื่อมต่อในซีรีส์ - บวกหนึ่งถึงลบของถัดไป ในกรณีนี้แรงดันไฟฟ้าจะถูกสรุปกระแสไฟฟ้ายังคงเหมือนเดิม
เริ่มกันเลย
หลังจากเลือกจำนวนตัวยึดสังกะสีที่ต้องการตามความยาวที่ต้องการเราพบลวดทองแดงที่เหมาะสม เป็นขดลวดในฉนวนวานิช เส้นผ่านศูนย์กลางของเส้นลวดประมาณ 0.5 มม.

เสาทำความสะอาดฉนวนวานิชหลายครั้งด้วยความพยายามดึงลวดผ่านผิวพับสองเท่าขนาดกลาง


จากนั้นเขาเตรียมขั้วไฟฟ้าหนึ่งคู่ - ไว้ใต้หัวสกรูที่ยึดตัวเองได้แนบสายไฟสองหรือสามรอบอย่างแน่นหนาแล้วตัดส่วนที่เกินออก

ชุดแบตเตอรี่ - รางถูกใช้เป็นภาชนะบรรจุน้ำแข็งแช่แข็ง คุณสามารถใช้เซลล์จากขนมชนิดบรรจุกล่องได้ แต่เซลล์เหล่านี้บอบบางกว่า หลังจากติดตั้งอิเล็กโทรดบนผนังระหว่างเซลล์แล้วเราเติมอิเลคโตรไลต์ลงในภาชนะ เราใช้วิธีแก้ปัญหาเกลือแกง - ช้อนโต๊ะกับน้ำอุ่น 0.5 ลิตร สำหรับการกรอกจะสะดวกมากที่จะใช้เข็มฉีดยาทางการแพทย์


เราพบสกรูอีกสองสามตัวสำหรับขั้วไฟฟ้าและเพิ่มส่วนประกอบเข้ากับแบตเตอรี่นั่นคือสิ่งที่เราได้รับ แรงดันไฟฟ้าที่โหลดความต้านทานสูง (ความต้านทานอินพุตของโวลต์มิเตอร์แบบดิจิตอล) มีความสำคัญมาก แต่ที่ภาระใด ๆ แต่ที่สังเกตเห็นได้ก็จะลดลงอย่างมีนัยสำคัญ
ลองทำดู เซลล์ไฟฟ้า (แบตเตอรี่) ที่คล้ายกันที่มีขั้วไฟฟ้าขนาดใหญ่.
ในฐานะที่เป็นภาชนะเราใช้โถขนาดครึ่งลิตร (สอง) แผ่นของพื้นที่ที่สำคัญจะพอดีกับมัน ในฐานะที่เป็นอิเล็กโทรดเราจึงใช้ฟอยล์ทองแดงและสังกะสีซึ่งเป็นเศษแก้วจากโรงงาน "แห้ง" ที่ถูกแยกออกในระหว่างการผลิตกราไฟท์สำหรับ เคลือบทนไฟ.

เราทำความสะอาดส่วนที่เหลือของเกลือผลึกแห้งด้วยแปรงลวดและตัดสองแผ่นด้วยกรรไกรโดยประมาณด้วยพื้นที่ประมาณเดียวกัน จากฟอยล์ทองแดงตัดสองลายเส้นที่ตรงกัน นอกจากนี้ยังมีกรรไกร เรามีอิเล็กโทรดสองคู่ซึ่งติดตั้งองค์ประกอบของเราโดยไม่ต้องกังวลใจต่อการดัดขอบของพวกเขาที่คอของกระป๋อง


ในภาชนะที่ใหญ่กว่าเราเตรียมอิเล็กโทรไลต์ - โซเดียมคลอไรด์ละลายในน้ำอุ่นความเข้มข้นจะเท่ากันและเทองค์ประกอบที่เตรียมไว้แล้วเท


เราเชื่อมต่อสององค์ประกอบในซีรีส์โดยใช้ชิ้นส่วนของสายยึดและคลิปจระเข้สองอัน ดังนั้นแรงดันไฟฟ้าของแบตเตอรี่อยู่ใกล้กับ "นิ้ว" มาตรฐานลองใช้ องค์ประกอบหนึ่งที่มีแรงดันไฟฟ้า 1.5 V ถูกใช้ในนาฬิการะบบเครื่องกลไฟฟ้านอกจากนี้การใช้งานนาฬิกาในปัจจุบันมีขนาดเล็กมากและแบตเตอรี่ของเราจะสามารถเอาชนะได้

เราถอดแบตเตอรี่มาตรฐานออกจากนาฬิกาและเชื่อมต่อกับขั้วต่อสายไฟหนึ่งชิ้น การสังเกตขั้ว (แผ่นทองแดง - "+", สังกะสี - "-"), เชื่อมต่อนาฬิกากับแบตเตอรี่ชั่วคราว, voila! นาฬิกาทำงานแรงดันไฟฟ้า "อ่างล้างมือ" ถึง 1.3 V นาฬิกาทำงานอย่างสมบูรณ์แบบเป็นเวลาหลายชั่วโมงจนกระทั่งเราทุกคนโอ้อวด (อย่างไรก็ตามนักมายากล!) จากนั้นเราก็เหนื่อย

เพื่อติดตาม
รัฐธรรมนูญภายในของเด็กคนใดที่ให้ความสนใจในเรื่องใดเรื่องหนึ่งเขาสามารถที่จะโฟกัสได้ไม่เกิน 15 ... 20 นาทีและทุกชั้นเรียนที่มีเด็กควรได้รับการวางแผนเพื่อที่พวกเขาจะได้พอดีในเวลานั้นหรือสลับระหว่างชั้นเรียนอื่น ๆ
ในฐานะที่เป็นโหลดจะดีกว่าที่จะใช้ว่าไม่ว่าจะเคลื่อนไหวหรือส่องสว่าง - ตัวเลขบนโวลต์มิเตอร์จะสร้างความประทับใจในใจ แต่ไม่ใช่หัวใจ นอกเหนือจากนาฬิกาและเครื่องคิดเลขแล้วมันจะทำให้เกิดความชื่นชมอย่างแน่นอนการทำงานจากแบตเตอรี่ที่ทำเองที่บ้านของเครื่องรับวิทยุขนาดเล็ก (เป็นตัวเลือก - ทำที่บ้าน!)
สำหรับการใช้งานในระยะยาวอิเล็กโทรไลต์ของเซลล์ควรได้รับการปกป้องจากฝุ่นละอองและการระเหยและดูแล depolarizer - อย่างน้อยอุดตันขวดด้วยแผ่นฟิล์มพลาสติกที่มีแถบยางยืดและเพิ่มโพแทสเซียมเปอร์แมงกาเนตกับอิเล็กโทรไลต์ ยิ่งไปกว่านั้นการรวบรวมองค์ประกอบที่กล่าวถึงใน Popov ทันที
นอกเหนือไปจากสกรูที่แตะตัวเองแล้วชุบสังกะสีมันเป็นไปได้ที่จะใช้แผ่นเหล็กชุบสังกะสีสำหรับองค์ประกอบขนาดใหญ่ที่สะดวกมากขึ้น - ในระหว่างการทดลองคุณจะได้รับกระแสไฟฟ้าและพลังงานที่สำคัญทุกอย่าง
รายชื่อวรรณกรรมที่ใช้แล้ว
1. P. Strelkov รู้และสามารถ วิศวกรไฟฟ้าผู้บุกเบิก Detgiz พ.ศ. 2503
2. V. Polosin, V.G. Prokopenko การประชุมเชิงปฏิบัติการเกี่ยวกับวิธีการสอนเคมี มอสโก, "การตรัสรู้", 1989, pp. 202,203

